Met een ionische vloeistof kun je selectief de zeldzaamste zeldzame aarden extraheren uit tl-buizen en spaarlampen. Dat maakt de recycling van deze afvalstroom ineens een stuk eenvoudiger, claimen de Leuvense onderzoekers David Dupont en Koen Binnemans in het tijdschrift Green Chemistry.
Zulke lampen bevatten een mix van fluorescentiepoeders, ‘fosforen’, die rood, groen en blauw licht geven. Die poeders bevatten alledrie zeldzame aarden maar in de ‘rode fosfor’ (niet te verwarren met de gelijknamige vorm van elementaire fosfor, want die heeft er niets mee te maken) is de concentratie verreweg het hoogst. Bovendien zijn de hierin verwerkte elementen, yttrium en europium, zelfs voor zeldzame aarden relatief schaars.
Recyclen ligt dus voor de hand. Alleen lossen die poeders nogal moeilijk op. Bij het grootste deel van het lampen-afval is nog nauwelijks sprake van recycling - het kwik wordt er uit gehaald vanwege de toxiciteit, maar de rest belandt op de stort. Voor zover Dupont en Binnemans weten, beschikt tot nu toe alleen chemieconcern Solvay over een terugwinningsproces voor de zeldzame aarden dat op industriële schaal functioneert. Maar dat is erg ingewikkeld, vertrouwt op grote volumes sterke zuren en basen en produceert een navenante hoeveelheid afval.
Het idee om die zeldzame aarden selectief op te lossen in een ionische vloeistof, dus een zout dat bij kamertemperatuur vloeibaar is, is op zich niet nieuw. Maar in Leuven hebben ze voor het eerst zo’n ionische vloeistof weten te vinden die de rode fosfor wél oplost en de minder waardevolle c.q. vrijwel waardeloze componenten van de poedermix ongemoeid laat.
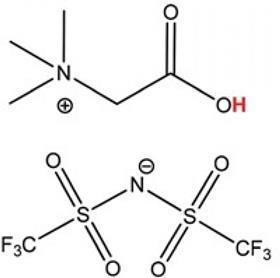
Het vloeibare zout wordt omschreven als betainium bis(trifluormethylsulfonyl)imide, afgekort [Hbet][Tf2N]. Het wordt omschreven als ‘gefunctionaliseerd’: het Hbet-kation reageert als Brønstedzuur en doet dat heftig genoeg om oxides van zeldzame aarden en de meeste overgangsmetalen op te lossen. Het Tf2N-anion zit erbij omdat je nu eenmaal een anion nodig hebt, maar verder doet het niets.
In de praktijk is de rode fosfor (Y2O3:Eu3+) de enige fractie die snel oplost in dit zure milieu. De overige fosforen lossen liever op in loog en de aluminium- en siliciumoxides in het afval lossen helemaal niet op. Wat wél een beetje oplost zijn de halogeenfosfaten (wél met het element fosfor!) die er vaak doorheen zitten, maar dat kun je tegengaan door de procescondities handig in te stellen. 24 uur sudddren bij 90 graden Celsius lijkt voorlopig het beste te werken; de auteurs stellen voor om er microgolven voor te gebruiken, zodat je de verhitting nauwkeurig in de hand hebt..
De Vlamingen stellen voor om het fijngemalen afval te dispergeren in de ionische vloeistof. Na een tijdje centrifugeer je de onopgeloste fractie af. Vervolgens voeg je oxaalzuur toe, zodat yttrium- en europiumoxalaten ontstaan die in deze ionische vloeistof onoplosbaar zijn. Deze neerslag filter je af, waarna je de ionische vloeistof opnieuw kunt gebruiken. Door verhitting tot 950 graden Celsius kun je tot slot die neerslag weer omzetten in zuiver Y2O3:Eu3+ dat zó weer de volgende tl-buis in kan.
Van alle ingrediënten kun je dus alleen dat oxaalzuur niet hergebruiken, en dat zijn de kosten niet. Bovendien produceer je in het geheel geen afvalwater en ook geen luchtvervuiling: ionische vloeistoffen verdampen immers niet.
Voorlopig werkt het overigens alleen in het lab. Over plannen om het proces op te schalen is nog niets bekend.
bron: KU Leuven















Nog geen opmerkingen