Vervang één waterstofatoom in insuline door jodium, en de stof kan veel sneller door het lichaam worden opgenomen. Het bewijst vooral dat je zulke trucjes ook kunt uithalen met eiwitten en niet alleen met kleine moleculen, schrijven onderzoekers uit Cleveland en Basel in het Journal of Biological Chemistry.
Door de wijziging vallen insulinehexameren (dus klontjes van zes insulinemoleculen) gemakkelijker uit elkaar. Die hexameren zijn inactief en dienen om insuline tijdelijk op te slaan in het lichaam; losse insulinemoleculen zijn daar veel te reactief voor. Het opsplitsen van hexameren kost echter tijd, en dat is de reden dat insuline-injecties voor diabetici ook niet direct werken.
Het idee die hexameren te destabiliseren om injecties sneller te laten werken, is zeker niet nieuw. Er zijn al meerdere van zulke insuline-analogen op de markt. Maar tot nu toe ontstonden ze allemaal door vervanging van complete aminozuren in de eiwitketen door andere natuurlijke aminozuren.
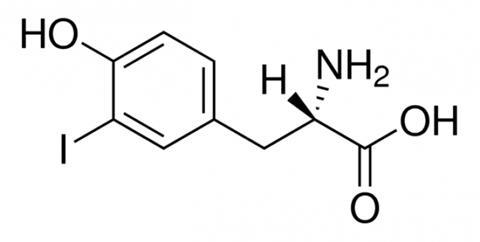
Michael Weiss (Case Western Reserve University) en collega’s laten nu zien dat het ook kan door één atoom in een van die aminozuren te vervangen, waarmee ze dus eigenlijk een onnatuurlijk aminozuur creëren. Om precies te zijn veranderen ze tyrosine op plek 26 van de B-keten van insuline in 3-joodtyrosine.
Kwantumchemische berekeningen en simulaties voorspelden dat deze modificatie het gewenste effect op de hexameerstructuur zou moeten hebben. Met röntgenkristallografie en NMR is achteraf vastgesteld dat de voorspellingen klopten. Dat het insuline nog steeds past op de bijbehorende receptoren, en dat er aan de biologische functie dus niets verandert, klopt ook.
Weiss sluit niet uit dat zijn gemodificeerde insuline klinisch toepasbaar is. Maar hij ziet het zelf vooral als proof of principle. In de medicinale chemie is het heel gewoon om te spelen met halogeenatomen, maar tot nu toe probeerde men het alleen bij kleine moleculen. Dat het ook bij eiwitten werkt, is nieuw.
bron: Universität Basel















Nog geen opmerkingen