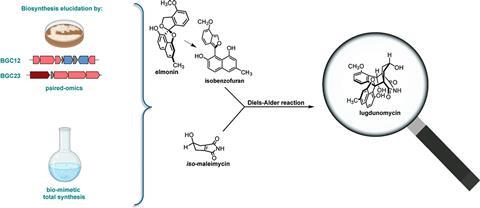
Door een hechte samenwerking tussen teams van de universiteiten van Leiden en Groningen is de totale synthese van het supercomplexe molecuul lugdunomycine gelukt en is de biosyntheseroute ervan opgehelderd, waarin een intermoleculaire Diels-Alder-reactie voorkomt. Ze hebben hun resultaten gepubliceerd in JACS.
Microben produceren de meeste medicijnen die je in de klinische praktijk gebruikt, waarvan 80% is gebaseerd op natuurlijke producten. Voorbeelden hiervan zijn penicilline, vancomycine en rapamycine. ‘Hoewel we geen nieuwe antibiotica lijken te kunnen ontdekken, is er nog veel onontgonnen chemisch terrein’, zegt hoogleraar Moleculaire Biotechnologie Gilles van Wezel. ‘Onze labs richten zich op het ontdekken van nieuwe geneesmiddelen die in dat gebied verborgen liggen.’
Ruim tien jaar geleden ontdekte de toenmalige promovendus Changsheng Wu een nieuwe, zeer complexe verbinding in de Streptomyces-stam QL37, genaamd lugdunomycine (naar de Latijnse naam voor Leiden, Lugdunum). ‘Ondanks de complexiteit tekende Wu de structuur bijna volledig correct op het whiteboard’, herinnert Van Wezel zich. ‘Maar zelfs met duizend agarplaten produceerden we slechts een paar honderd microgram – lang niet genoeg voor een uitgebreide analyse.’
Ontbrekend elektronenpaar
Op dat moment ging het NACTAR-programma van NWO-TTW van start, met onder meer het lugdunomycine-project, waarin onderzoekers uit Leiden en Groningen samenwerkten met industriële partners Pfizer, Batavia Biosciences (Leiden) en Fundacion Medina (Granada, Spanje).

‘Adri [Minnaard, hoogleraar organische chemie in Groningen] zei dat zijn groep de synthese van het molecuul onder handen zou nemen’, vertelt Van Wezel. ‘Ons doel was om het genetische pad van de biosynthese van lugdunomycine te begrijpen.’ Wu had niet alleen de structuur vrijwel perfect voorspeld, maar ook het biosynthetische pad. ‘Maar er ontbrak één elektronenpaar. Michiel en Isabel kregen de taak om dit probleem op te lossen.’ Michiel Uiterweerd, promovendus in het lab van Minnaard, nam de chemische synthese voor zijn rekening, terwijl Isabel Nuñez Santiago, promovendus in de groep van Van Wezel, zich richtte op de genetica en het biosyntheseroute.
‘De realisatie kwam na lang puzzelen en het verwoed tekenen van structuren’
Michiel Uiterweerd
‘Toen Adri me de molecule liet zien, was ik meteen verkocht. Ik wilde het maken!’, zegt Uiterweerd. Op dat moment was het duidelijk dat een cruciale stap in de synthese van lugdunomycine een intermoleculaire Diels-Alder-reactie was, waarbij een dieen reageert met een diënofiel. ‘Vanuit biochemisch perspectief dachten we eerst aan maleimycine als kandidaat-dieen.’ Maar vanuit retrosynthetisch perspectief zou dat een Diels-Alder-product opleveren met de alcohol op de verkeerde plaats.
‘We konden chemisch niet verklaren hoe de natuur de alcohol vervolgens zou “verplaatsen”, en we wisten ook niet hoe we dat in het lab konden bereiken’, gaat Uiterweerd verder. ‘Dus dachten we dat er een isomeer van maleimycine in het spel was, dat we iso-maleimycine noemden.’ Beide kandidaat-diënofielen werden in het lab gemaakt, en vervolgens ontdekten ze dat iso-maleimycine werd geproduceerd door de QL37-stam, waardoor dit de voornaamste kandidaat werd.
Nachtmerrie
Met een ruw idee van de diënofiel gingen ze verder met het dieen. ‘Op een dag vond Helga van der Heul, een andere promovendus uit de Van Wezel-groep, een gepubliceerd molecuul met een structureel element dat ook in lugdunomycine voorkomt’, zegt Uiterweerd. Dit was elmonine, een bekende herschikte angucyclinon uit Streptomyces. ‘Op dat moment wisten we gewoon niet of de QL37-stam het ook produceerde. Na lang puzzelen en het verwoed tekenen van structuren, realiseerde ik me dat elmonine veel lijkt op veelvoorkomende isobenzofuran-precursormoleculen. En die isobenzofuranen zijn zeer reactieve diënen in Diels-Alder-reacties!’ De hypothese die hieruit voortkwam was dat elmonine een gemaskeerde isobenzofuran is, die als dieen zou kunnen fungeren.
‘Per toeval ontdekte ik dat je lugdunomycine ook in vloeibare culturen kunt produceren’
Isabel Nuñez Santiago
Nadat ze elmonine met succes hadden gesynthetiseerd en de reactieomstandigheden hadden bepaald die nodig waren om het te laten reageren met iso-maleimycine, stuitten ze op de nachtmerrie van alle organisch chemici: ‘Toen we het NMR-spectrum van onze verbinding vergeleken met dat van lugdunomycine, zagen we alle pieken, maar ze hadden verschillende chemische verschuivingen. Het bleek dat we een isomeer van lugdunomycine hadden gemaakt.’ Na kristallografische analyse ontdekten ze dat het om het C9-epimeer ging. ‘De Diels-Alder-reactie werkte zoals verwacht, maar we kregen een ander diastereomeer dan in de natuur voorkomt.’

Lipases
Ondertussen gaf theoretisch chemicus Remco Havenith met behulp van computers inzicht in de verschillen tussen de mogelijke reactiepaden. Het werd duidelijk dat de energieverschillen tussen de reactiebarrières en de afzonderlijke isomeren niet zo groot waren.
‘Daardoor vermoedden we dat er bij de natuurlijke reactie een externe factor betrokken moet zijn die de reactie stuurt’, vervolgt Uiterweerd. Door wat niet-verwante eiwitten aan het reactiemengsel toe te voegen, ontdekten ze dat sommige lipasen de stereoselectiviteit iets veranderden in het voordeel van lugdunomycine en, tot hun verrassing, de Diels-Alder-reactie konden katalyseren. ’Uiteindelijk kon ik de reactie opschalen, de diastereomeren scheiden en de moleculen isoleren. Dit toonde aan dat iso-maleimycine en elmonine inderdaad de bouwstenen waren voor lugdunomycine in QL37.’
Keerpunt
Het vinden van de oorsprong van deze bouwstenen was de uitdaging voor Nuñez Santiago. Ze bouwde voort op het werk van twee eerdere promovendi, Helga van der Heul en Xiansha Xiao, die zich vooral hadden gericht op de genetische componenten die volgens het Leidse team verantwoordelijk waren voor de productie van lugdunomycine. ‘Maar toen onze collega’s in Groningen iso-maleimycine synthetiseerden, konden we die verbinding ook gebruiken om ernaar te zoeken in het metaboloom’, legt Nuñez Santiago uit. ‘Dat was een keerpunt voor het project.’
‘Het project was misschien niet makkelijk, maar wel heel leuk!’
Gilles van Wezel
‘In eerste instantie probeerden we lugdunomycine te produceren in vloeibare culturen, maar dat leek alleen te werken op vaste agarplaten’, vertelt Nuñez Santiago. ‘Maar toevallig ontdekte ik dat het wel werkte in vloeibare vorm als je galactose als belangrijkste koolstofbron gebruikt.’ Tijdens proteoomonderzoek ontdekte ze eiwitten die actief werden wanneer je de bacterieculturen in galactose kweekt.
Het bleek dat niet één, maar twee biosynthetische genclusters verantwoordelijk waren voor de biosynthese van de bouwstenen, en die lagen behoorlijk ver uit elkaar in het genoom. ‘Het is heel zeldzaam dat zulke clusters zo ver uit elkaar liggen en toch deel uitmaken van hetzelfde biosynthetische proces!’
Uitzondering
Lugdunomycine is een supercomplex molecuul dat in meerdere bacteriesoorten voorkomt. Maar wat doet het eigenlijk? ‘Dat weten we gewoon niet’, geeft Van Wezel toe. ‘Het is maar een mild antibioticum, dus de echte functie blijft een raadsel.’ Volgens de Leidse professor richt zijn groep zich zelden op afzonderlijke moleculen, omdat ze vooral bezig zijn met het vinden van nieuwe manieren en technologieën om antibiotica te ontdekken. ‘Maar lugdunomycine is een uitzondering. Ik wil gewoon weten wat het doet. Waarom zou een microbe zoveel tijd en moeite steken in zo’n ingewikkelde synthese?’
Iedereen waardeerde de samenwerkingen. ‘Voor de studenten is dit een groot voordeel: samenwerken met het bedrijfsleven, met andere disciplines en je netwerk uitbreiden. Ik vind dit soort projecten ook leuker.’ Het uiteindelijke artikel bestaat in wezen uit twee verschillende verhalen, zegt Nuñez Santiago. ‘Het was waardevol om de belangrijkste overeenkomsten te identificeren en sessies te houden over het overkoepelende verhaal.’
Twee vs. één
Hoe gaat dit werk het onderzoek naar antibiotica helpen? ‘Volgens mij draait het allemaal om kennis’, zegt Núñez Santiago. ‘Het is een goed voorbeeld van hoe we buiten de gebaande paden moeten denken en naar andere vakgebieden moeten kijken om samen te werken. Er valt nog heel veel nieuwe chemie te ontdekken.’
Van Wezel hoopt dat het werk anderen zal inspireren. ‘Er zijn veel manieren om nieuwe medicijnen te vinden, vaak met behulp van microbiologie. Hier hebben we een nieuwe aanpak laten zien. Normaal gesproken neem je de biosynthetische genclusters, zet je die in een geoptimaliseerde gastheer en forceer je de expressie van één cluster om een molecuul te produceren. Maar voor lugdunomycine werkte deze aanpak niet, omdat je twee clusters nodig hebt. Sindsdien hebben we meerdere voorbeelden gevonden van moleculen die twee clusters nodig hebben, dus als je er maar één gebruikt, mis je veel chemie.’
‘Dit geeft ook veel inzicht in de secundaire stofwisseling’, zegt Uiterweerd. ‘Er is veel activiteit in deze stofwisseling. Als je nieuwe antibiotica wilt ontdekken, moet je deze processen begrijpen.’ Van Wezel voegt toe: ‘Lugdunomycine is een angucycline, de grootste familie van natuurlijke producten. Met dit project hebben we onze kennis over de biosynthese van deze verbindingen aanzienlijk uitgebreid en veel nieuwe chemische inzichten opgedaan. Het was misschien niet gemakkelijk, maar het was wel heel leuk!’
Uiterweerd, M.T., Nuñez Santiago, I. et al. (2025) JACS 147(16), DOI: 10.1021/jacs.5c01883
Uiterweerd, M.T., Nuñez Santiago, I. et al. (2025) JACS 147(16), DOI: 10.1021/jacs.5c01883Intermoleculaire Diels-Alder is laatste stap in supercomplexe natuurstof




















Nog geen opmerkingen