Nieuwe antibiotica zijn broodnodig, maar zolang de markt niet verandert, maken veelbelovende ontwikkelingen geen schijn van kans. Investeren in iets wat je hopelijk niet nodig hebt is altijd een tough sell.
Een sluimerende pandemie, zo wordt de toename van het aantal resistentie-infecties wel omschreven. Nu al sterven jaarlijks 700.000 mensen wereldwijd aan de gevolgen van een resistente, voornamelijk bacteriële infectie. Een infectie waartegen geen enkel middel nog werkt. Als we niets doen, loopt dat aantal op tot tien miljoen in 2050, volgens prognoses van de Wereldgezondheidsorganisatie (WHO).
Tegelijkertijd neemt het aantal nieuwe antimicrobiële middelen (dus tegen bacteriën, virussen en schimmels) dat op de markt komt al jaren af. Een vreemde tegenstelling, want de ‘unmet medical need’ waar bedrijven en investeerders in de farma- en biotechindustrie zo graag mee schermen, lijkt evident. Toch zijn er in clinicaltrials.gov, het internationale overzicht van klinische studies, meer dan 80.000 studies te vinden gerelateerd aan kanker tegenover slechts 6.600 studies gericht op (resistente) bacteriële infecties. Waarom blijft de ontwikkeling van nieuwe antibiotica zo mijlenver achter?
Niet lucratief
‘Het is duidelijk dat de markt faalt als aanjager van nieuwe antibiotica’, zegt Nathaniel Martin, hoogleraar biologische chemie aan de Universiteit Leiden. ‘Er zijn de afgelopen decennia verschillende initiatieven ontplooid om onderzoek naar nieuwe antimicrobiële middelen te financieren, maar de huidige markt nodigt totaal niet uit om te investeren in antibiotica R&D.’
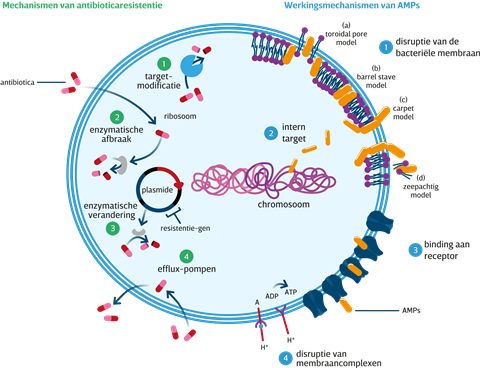
Hij krijgt bijval van Remko van Leeuwen, oprichter van Madam Therapeutics, een Nederlandse ontwikkelaar van antimicrobiële peptiden (AMP; zie illustratie) tegen moeilijk behandelbare bacteriële infecties. ‘Er zijn ook problemen aan de wetenschappelijke kant, maar het grootste probleem zit toch echt bij de markt.’ In de huidige markt geldt: hoe meer een middel wordt voorgeschreven, hoe hoger de inkomsten. Maar voor nieuwe antibiotica is dat nou net niet de bedoeling, want die willen we zo min mogelijk inzetten om resistentie te voorkomen. Maar welk bedrijf gaat honderden miljoenen investeren om een geneesmiddel te ontwikkelen dat vervolgens juist niet wordt gebruikt, lees: verkocht? De grote farmabedrijven niet, zij kiezen voor lucratievere gebieden.
Het overgrote deel van de antimicrobiële R&D komt voor rekening van kleine bedrijven als Madam Therapeutics. Voor die bedrijven is het ontzettend moeilijk om financiering te vinden voor het klinische onderzoek. ‘Meer dan moeilijk, zeg maar gerust onmogelijk’, reageert Van Leeuwen. ‘In 2014 was er nog een interessante deal in de markt, de overname van Cubist door Merck voor € 9 miljard, maar sindsdien is het helemaal opgedroogd. Als er nog deals zijn, praten we over honderd miljoen of zelfs minder. Dat stelt in de farma-industrie niets voor. Het geeft aan hoe laag de waardering is voor de ontwikkeling van nieuwe antibiotica.’
‘Het is duidelijk dat de markt faalt als aanjager van nieuwe antibiotica’
Nathaniel Martin
Niet te verkrijgen
Het wrange is dat zelfs bedrijven die het wel lukt om de sprong naar klinisch onderzoek te maken en daar goede resultaten laten zien en in sommige gevallen het zelfs tot marktoelating weten te brengen, hun leven niet zeker zijn. Van de vijftien nieuwe antibiotica die in de jaren 2010-2019 zijn goedgekeurd door de Amerikaanse FDA zijn er vijf niet of nauwelijks te verkrijgen, omdat de desbetreffende bedrijven ondertussen failliet zijn gegaan of niet meer over de mensen en middelen beschikken om de productie te verzorgen.
Goedgekeurde middelen die in een soort schemergebied zweven. Dat is niet alleen frustrerend voor de betrokken bedrijven en onderzoekers, het vormt ook een grote zorg, aldus een rapport van de Access to Medicine Foundation uit 2021. Want als de bedrijven die ons moeten beschermen tegen superbugs – de resistente ziekteverwekkers – zichzelf niet kunnen redden, dan komen die nieuwe geneesmiddelen er nooit.
Al deze problemen zijn natuurlijk al veel langer bekend. Toch lijkt er nu wat beweging in het veld te ontstaan om dit niet langer lijdzaam aan te zien. In 2016 lanceerde Boston University CARB-X, een non-profit accelerator die inmiddels ruim $ 350 miljoen in (pre)klinisch onderzoek bij kleine bedrijven heeft gefinancierd. In 2020 kwam het AMR Action Fund van de grond, een internationaal consortium van grote farmabedrijven en publieke organisaties, dat een $ 1 miljard wil investeren, zodat er in 2030 twee, drie of vier nieuwe antibiotica op de markt komen.
Van Leeuwen is gematigd positief. ‘Een mooi initiatief, maar zij pakken een project pas op na fase 1 (het klinisch onderzoek in gezonde vrijwilligers, red.) en daarvoor zijn er ook nog veel problemen. Bovendien, $ 1 miljard is een mooi bedrag en het is bemoedigend dat grote farmabedrijven hieraan bijdragen, maar als je dat afzet tegen wat er in deze sector omgaat, is het natuurlijk heel weinig. Alleen Pfizer heeft naar eigen zeggen al $ 2 miljard vrijgemaakt voor de ontwikkeling van hun coronavaccin. Dat was voor slechts één product.’
Ook Martin reageert terughoudend. ‘Het AMR Action Fund is een goede start, maar zonder verdere veranderingen in de markt gaat het niet werken. Dat geldt ook voor CARB-X. Dat heeft wel geleid tot goedgekeurde middelen, maar die bedrijven zijn toch nog omgevallen.’
De doorbraak ligt volgens Martin in een nieuwe visie op de rol en het belang van antibiotica in de gezondheidszorg. ‘Antibiotica zijn geen geneesmiddelen die zijn gericht op een specifieke ziekte van een individuele patiënt, maar ze zijn onderdeel van de grotere infrastructuur. Heel veel operaties kun je simpelweg niet uitvoeren als je geen antibiotica voorhanden hebt. Ik vergelijk ze vaak met zoiets als bedden. Niemand vindt het vreemd dat een ziekenhuis nieuwe bedden aanschaft. Zo moeten we ook naar antibiotica gaan kijken, die heb je gewoon nodig om een ziekenhuis te laten functioneren.’
‘Als er nog deals zijn, praten we over honderd miljoen of zelfs minder; dat stelt in de farma-industrie niets voor’
Remko van Leeuwen
Netflix-model
Het publieke belang van antibiotica moet voorop komen te staan, vindt ook Van Leeuwen. ‘Er is een groot belang voor de volksgezondheid om resistentie te voorkomen en voldoende werkzame antibiotica achter de hand te hebben. We moeten waarde creëren in het ontwikkelen van antibiotica en de overheid moet daarin een sturende rol op zich nemen.’
Ook op dat front wordt, buiten Nederland, bewogen. Verschillende landen, waaronder Zweden, de VS en het VK, experimenteren met nieuwe vergoedingssystemen voor antibiotica. Zoals het Netflix-model, dat werkt met abonnementen: fabrikanten ontvangen een vast bedrag, los van hoeveel daadwerkelijk wordt gebruikt. Een andere optie is om bedrijven een vergoeding te bieden op het moment dat een nieuw middel is goedgekeurd. Allemaal strategieën om de ontwikkeling van antibiotica te belonen in plaats van de inkomsten volledig te laten bepalen door de verkochte volumes. Dat vraagt dus om publieke investeringen, zodat we het ons kunnen veroorloven om kostbare, nieuwe antibiotica op de plank te leggen. Investeren in iets wat je hopelijk niet nodig hebt is altijd een tough sell.
‘Het probleem van antimicrobiële resistentie wordt wel onderkend door de overheid, maar de noodzaak tot concrete actie ontbreekt’, zegt Van Leeuwen. Deels begrijpt hij dat wel. ‘We moeten eerlijk zijn, hier valt het resistentieprobleem nog mee, maar wereldwijd zeker niet.’ De coronapandemie heeft mensen wel wakker geschud. ‘Het is nu duidelijk dat infectieziekten niet iets zijn uit het verleden, waar wij hier in het rijke Westen geen last meer van hebben. De politiek is nu meer bereid om te investeren zodat we beter voorbereid zijn op nieuwe problemen met infectieziekten. Dat kan helpen om het resistentieprobleem serieus onder ogen te zien.’
Maar het blijft een lastig verhaal, zegt Martin. ‘Er is nu meer maatschappelijke en bestuurlijke aandacht voor de dreiging van infectieziekten, maar het blijft moeilijk om een ministerie te overtuigen van de noodzaak tot investeren in een oplossing voor een probleem dat er nog niet is. We zijn hier nog niet op het punt gekomen dat artsen geen enkele optie meer hebben om bacteriële infecties te behandelen en dus is er ook nog geen keiharde noodzaak om actie te ondernemen.’
Tanks
Desondanks zou de overheid volgens Martin al stappen kunnen zetten om het denken over antibiotica te veranderen. ‘Begin eens met discussies over het de-risken van antibiotica-ontwikkeling. Ga praten met verzekeraars en andere partijen over wat een mogelijke financiële vergoeding zou kunnen zijn voor een bedrijf dat een nieuw middel ontwikkelt aan de hand van een set voorwaarden.’
Martin ziet parallellen met andere publieke projecten op basis van aanbestedingen. ‘Als het Ministerie van Defensie nieuwe tanks nodig heeft, dan stellen ze een lijst met eisen en kijken vervolgens welk bedrijf de gewenste tank kan leveren. En die tanks worden misschien nooit ingezet in een oorlog. Zo kun je ook naar nieuwe antibiotica kijken. Stel, Nederland wil X miljoen besteden aan een nieuw middel. De volgende stap is dan praten met andere landen en als die ook een X bedrag willen vrijmaken, dan gaat het lopen en wordt het voor een bedrijf interessant om hieraan te gaan werken. Denk in ieder geval eens over die mogelijkheid na.’



















Nog geen opmerkingen