Eicellen bevatten een groot aantal eiwitten om te helpen bij embryonale ontwikkeling. Ze bewaren deze voorraad in specifieke opslagcomplexen, maar hoe die er precies uitzien was onduidelijk. In Nature presenteren onderzoekers van het Hubrecht Instituut deze ‘eiwitkasten’ nu van dichtbij.
Tijdens de menstruatiecyclus rijpt een onrijpe eicel, een oöcyt, uit tot een volwaardige eicel; een van de grootste cellen in het vrouwelijk lichaam. Om deze enorme transformatie mogelijk te maken hoopt de oöcyt een groot aantal eiwitten en andere moleculen op. In de jaren zestig ontdekten wetenschappers dat oöcyten ook grote vezelachtige structuren bevatten, zogeheten cytoplasmatische roosters, maar hun functie bleef een punt van discussie. Een doorbraak volgde in 2023, toen het team van celbioloog Melina Schuh van het Max Planck Institute for Multidisciplinary Sciences liet zien dat deze roosters als opslagsysteem dienen voor veel van de eiwitten die cruciaal zijn voor embryonale ontwikkeling.
Waar de opslagcomplexen uit bestaan en hoe ze georganiseerd zijn, bleef nog onduidelijk. Nu presenteert de groep van structuurbioloog Miguel Leung van het Hubrecht Instituut in Utrecht hun structuur in muis-oöcyten met ongekend detail. Ze laten bovendien zien hoe alle eiwitten in elkaar passen tot het complex. Hun paper staat niet op zichzelf. Twee andere publicaties in Nature en drie preprints komen tot dezelfde structuur, allemaal bepaald in muis-oöcyten, -eicellen en -embryo’s uit verschillende stadia. Volgens Leung is het geen toeval dat zes onderzoeksgroepen op hetzelfde moment tot dit resultaat convergeren: ‘Dankzij de vooruitgang in de structurele biologie, zoals verbeteringen in cryo-EM en beeldverwerking, hebben we nu dit resultaat kunnen bereiken.’
[Lees verder onder de afbeelding]
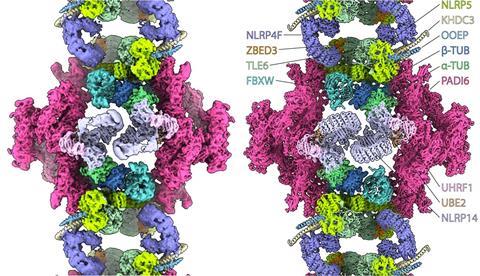
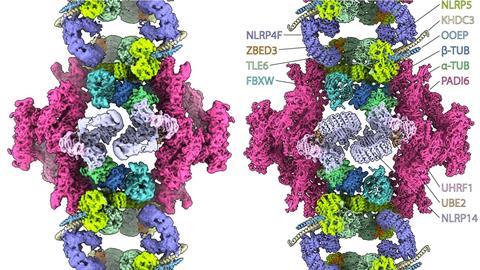
Tubuline-opslag
Tot hun verbazing ontdekten de onderzoekers dat sommige eiwitten in de cytoplasmatische roosters ubiquitinatiefactoren zijn – enzymen die de afbraak van eiwitten reguleren. Wat deze eiwitten daar doen, is nog niet duidelijk. ‘Misschien dat eiwitniveaus hierdoor kunnen toenemen in de oöcyt’, zegt Leung. ‘Stel dat deze factoren vrij zouden rondzweven, dan kunnen ze eiwitten taggen die daardoor afgebroken worden terwijl dat niet de bedoeling is. Door ze bijeen te houden in het cytoplasmatisch rooster, kan dit de oöcyt helpen om een grote verzameling eiwitten op te bouwen.’
Een andere onverwachte ontdekking is dat de roosters tubuline bevatten, een eiwit dat helpt bij de opbouw van het celskelet en het transport van materialen binnen de cel. ‘Tubuline is nog nooit eerder in deze vorm gezien in een eiwitcomplex in eender welk celtype. Onze hypothese is dat de tubuline later losgelaten kan worden om snel te polymeriseren tot microtubuli voor de vele celdelingen in het embryo.’
Cel openbreken
Om de cytoplasmatische roosters visueel uit elkaar te pluizen, maakten de onderzoekers gebruik van cryo-EM. Hiervoor werkten ze samen met cryo-EM deskundige Willem Noteborn van het Netherlands Centre for Electron Nanoscopy. De uitdaging zat erin dat een oöcyt (~100 micrometer) vele malen groter is dan de dikte van een cryo-EM-sample (~100 nanometer). Leung: ‘De truc was om de oöcyt open te laten barsten met een detergent, de inhoud snel uit te spreiden over het EM-rooster en dit direct te bevriezen.’
Tussen de rommelige celinhoud zochten de onderzoekers vervolgens met de microscoop naar de cytoplasmatische roosters, die door hun grootte duidelijk te herkennen waren. Ze legden 40.000 filmpjes vast, waarmee ze konden laten zien dat het cytoplasmatisch rooster uit minstens dertien verschillende eiwitten bestaat, waarvan veel zelf een cruciale rol spelen in embryonale ontwikkeling. De eiwitkast bleek dus opgebouwd uit de opgeslagen eiwitten zelf.
Als bevestiging werkten de onderzoekers samen met het Proteomics team van het Centre for Molecular Medicine van het UMC Utrecht. Met massaspectrometrie toonden zij aan dat de eiwitten in de cryo-EM reconstructie ook in grote hoeveelheden in de oöcyten voortkomen.
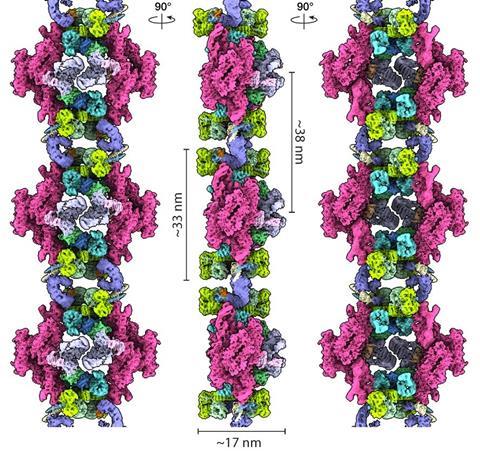
Evolutie
Als volgende stap willen de onderzoekers achterhalen hoe de complexe opslagstructuren assembleren. Hierbij is Leung met name gefascineerd door de verschillen tussen de roosters van verschillende organismen. ‘Alle zes publicaties laten de structuur van de roosters zien in een muis. Maar deze verschilt nogal met die van een mens. Zo is een van de eiwitten in het rooster van een muizenoöcyt niet aanwezig in de onze.’
Door de implicaties van dit soort verschillen te bepalen, hoopt Leung inzicht te krijgen in de verschillende mechanismen voor de vroege ontwikkeling van leven. ‘Veel van de eiwitten die belangrijk zijn in cytoplasmatische roosters bij zoogdieren komen niet eens voor in kikkers en vissen. Hoe ontwikkelen zij dan een embryo? Dit evolutionaire aspect vind ik zeer interessant.’
Kılıç, Z.I., van Loenhout, J., Chaillet, M. et al., Cytoplasmic lattices are megadalton storage complexes in mammalian oocytes, Nature (2026), doi:10.1038/s41586-026-10513-8



















Nog geen opmerkingen