Een Nijmeegs-Amsterdams team presenteert in Nature Chemistry een model-gestuurde strategie om op het juiste moment de juiste stoffen aan reactieketens toe te voegen. Deze tijdsafhankelijke doseerstrategie maakt het uitvoeren van complexe reacties niet alleen efficiënter, maar kan ze ook goedkoper maken.
De groep van Wilhelm Huck (Radboud Universiteit) ontwikkelde met Bob van Sluijs (Universiteit van Amsterdam) ontwerpstrategieën om de opbrengst van enzymatic reaction networks (ERN’s) te verhogen. Aan de hand van modellen bepaalden ze hoe en en vooral ook wanneer je stoffen in zulke systemen het beste kunt toevoegen voor een maximale opbrengst. Het werk verscheen op 6 mei in Nature Chemistry. Huck licht toe waar het idee voor dit onderzoek vandaan kwam: ‘Het besef dat er zoveel mogelijkheden zijn om de opbrengsten van complexe reacties te verbeteren door de factor tijd expliciet mee te nemen.’
Geen kinderspel
Een ERN bestaat typisch uit enzymen (de katalysatoren), substraten (de beginstoffen) en cofactoren zoals ATP (adenosinetrifosfaat) en omvat een multistaps organische syntheseroute, waarbij iedere stap een enzymatische conversie is. Dit kan als een one-pot-synthesis worden uitgevoerd, maar het is geen kinderspel om alle componenten vanaf het begin in de juiste concentraties samen te brengen voor een optimale opbrengst. Zo zijn veel enzymatische reacties omkeerbaar waardoor producten weer worden teruggevormd naar de beginstoffen. Ook concurreren verschillende reacties vaak om dezelfde cofactoren waardoor soms één reactieroute domineert terwijl andere stilvallen, of is er een tussenproduct dat één van de enzymen inhibeert.
Eindeloos veel recepten
Huck, Van Sluijs en collega’s onderzochten wat er gebeurt als je in een ERN niet alle ingrediënten tegelijk toevoegt, maar componenten op verschillende momenten doseert. Huck: ‘We vroegen ons af: wat nou als je op elk tijdstip kunt toevoegen wat je wilt?’ Daarmee stellen ze de klassieke batch-benadering (’alles mengen en wachten op steady-state’) op de proef. ‘We hebben laten zien dat je met tijdsafhankelijke toevoegingen het systeem naar een veel hogere opbrengst kunt sturen’, zegt Huck.
Om duidelijk te maken hoe belangrijk timing is in reactienetwerken, geven ze in hun paper een voorbeeld. Acht reactiecomponenten met elk tien mogelijke doseringen leveren al 108 combinaties op. Maar als je ook rekening houdt met wanneer componenten worden toegevoegd – bijvoorbeeld verdeeld over 24 tijdstappen – groeit dat aantal tot (108)24 mogelijke recepten.
De belangrijkste hypothese achter dit werk is dat er tussen die enorme hoeveelheid mogelijke doseerschema’s patronen zitten die je niet zomaar zou bedenken, maar die wel veel hogere opbrengsten geven. Die kun je alleen niet gewoon allemaal proberen: enzymen en cofactoren zijn daarvoor te duur en te schaars. Bovendien zijn de mogelijkheden bijna eindeloos.
‘We hebben laten zien dat je met tijdsafhankelijke toevoegingen het systeem naar een veel hogere opbrengst kunt sturen’
Wilhelm Huck
Doseerschema
Daar komt Van Sluijs’ strategie goed van pas. Allereerst liet hij een model bepalen welke experimenten je moet doen om het gedrag van een ERN zo efficiënt mogelijk te leren begrijpen en nauwkeurig te modelleren. Daarna gebruikte hij de data over hoe alle relevante chemicaliën in het reactienetwerk (substraten, tussenproducten, cofactoren en eindproducten) evolueren tijdens de reactie om meerdere wiskundige modellen van het systeem te trainen en te testen. Vervolgens koos hij het model dat de beste voorspellingen doet over welke stoffen je moet toevoegen, op welke momenten je dat moet doen en in welke volgorde en hoeveelheden. Oftwel: het doseerschema.
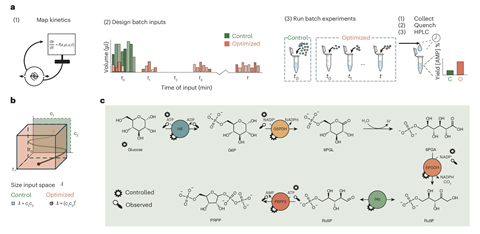
Huck en collega’s testten in een flowreactor twee enzymatische reactieketens (de pentosefosfaatroute en de nucleotide-recyclingroute) op twee manieren: met de klassieke alles-in-één-keer aanpak en met door het model geoptimaliseerde, tijdsafhankelijke doseerschema’s. Daarbij leverden de model-gestuurde schema’s duidelijk meer eindproduct op. In de pentosefosfaatroute werd ongeveer 5,7 keer meer AMP geproduceerd en steeg de omzetting van glucose naar product van circa 12% naar 48%. In de nucleotide-recyclingroute brachten de gespreide toevoegingen concurrerende reacties beter in balans, waardoor de opbrengst van UTP ongeveer 21 keer hoger uitviel dan bij de standaardaanpak.
Net als bakken
‘Het is net als met bakken,’ zegt Huck. ‘Je kunt in één keer alles door elkaar roeren, maar bij de meeste recepten moet je eerst mengen, kneden, nog wat toevoegen, alles laten rijzen en dáárna zet je het pas in de oven. Eigenlijk zeggen we nu: met deze methode kan ik je een recept geven. En als je dat volgt, krijg je een veel betere opbrengst.’
Hoe zit het met opschalen? ‘Dan zijn er extra parameters als roeren, massatransport en warmtetransport waar we in het model op dit moment geen rekening mee houden,’ zegt Huck. ‘Dan moet je het opschalen zélf denk ik zien als een tijdsafhankelijk recept. Moet je echt kilo’s roeren dan kun je hard of zacht roeren, snel in het begin en langzaam later. Die parameters kun je automatiseren. Maar op dit moment hebben we dat niet meegenomen.’
Een belangrijke volgende stap is formuleringen maken, aldus Huck. ’Dus van alle processtappen als mengen, roeren, schudden et cetera een tijdsafhankelijk recept maken. Dan ga je richting het optimaliseren van chemische technologie.’ Met Van Sluijs denkt hij erover om een bedrijf op te richten dat deze modellen op andere systemen kan toepassen. ‘Maar dan moeten mensen wel geïnteresseerd zijn in tijdsafhankelijk recepten,’ zegt Huck. ‘Daarvoor moeten wij meer voorbeelden hebben waarmee we laten zien dat we meerdere syntheseroutes of formuleringen kunnen optimaliseren.’
















Nog geen opmerkingen