Eiwitten hebben vaak een toepassing in medische behandelingen, maar toch zitten daar haken en ogen aan. Onderzoekers aan de UTwente hebben gekeken naar antilichaamfragmenten om een beter werkend alternatief te produceren. ‘Ze hebben een groot potentieel in de geneeskunde vanwege hun hoge specificiteit en werkzaamheid.’
De medische wereld maakt veel gebruik van eiwitten. Deze bieden verschillende mogelijkheden bij de behandelingen van kanker, infecties of metabolische stoornissen. De grote voordelen van het gebruik van eiwitten is de hoge bio-activiteit en de hoge specificiteit. Deze eigenschappen ontstaan door de complexe secundaire en tertiaire structuren die je niet terugvindt bij andere stoffen. Een nadeel dat aan eiwitten kleeft is dat enzymen ze in het lichaam afbreken.
Onderzoekers van de UTwente hebben nu gekeken naar single-chain heavy chain only antibody fragments, ook wel bekend als VHH’s, als alternatief. Deze moleculen zijn zeer stabiel en hebben een gemakkelijk en goedkoop productieproces. Hun korte halveringstijd is echter nog wel een nadeel. ‘VHH’s hebben een groot potentieel in de geneeskunde vanwege hun hoge specificiteit en werkzaamheid, maar vaak zijn ze, door hun lage molecuulgewicht, al na enkele uren uit het lichaam verwijderd’, zegt postodoctoral fellow Bram Zoetebier in een e-mail. Om deze reden is er veel onderzoek naar het koppelen van de VHH aan een polymeer. Dit verhoogt de halveringstijd en daarmee ook de tijd dat het VHH-molecuul actief is.
In Twente hebben ze zes verschillende VHH’s geproduceerd door middel van genetische modificatie. ‘Toen één VHH een zeer lage conjugatie-efficiëntie vertoonde, gaf dit de aanleiding tot verdere genetische aanpassingen’, zegt Zoetebier. Iedere VHH is gekoppeld aan een ongepaarde cysteïne in de C-terminal. Daarmee keken ze hoe goed deze moleculen in staat zijn om te binden aan polysachariden om zo een modulair en multivalent platform te maken. Hier testten ze twee verschillende varianten van: dextraanmaleïmide en hyaluronzuurmaleïmide.
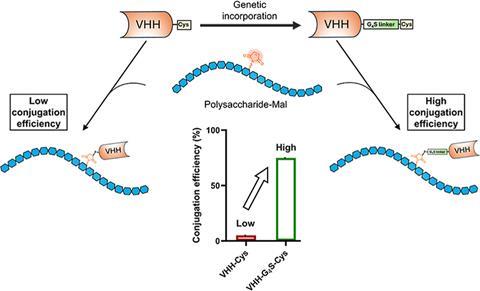
De onderzoekers vonden opmerkelijke verschillen in de conjugatie tussen de VHH’s, ongeacht aan welke polysachariden ze bonden. Sommige laten zelfs een conjugatie-efficiëntie zien van 70%. Maar voor één van de VHH’s, anti-TNFα-VHH-Cys, was dit niet het geval. Deze ondervond een lage conjugatie van maar 5%. Dat komt door de structurele heterogeniteit die invloed uitoefent op de reactiviteit van de Cys. Zoetebier en collega’s kozen ervoor om verder te kijken en G4S toe te voegen aan het eiwit. ‘G4S is een flexibele, goed wateroplosbare linker, waardoor de cysteïne goed beschikbaar is voor conjugatie.’ legt hij uit. Deze aanpassing verhoogde de conjugatie-effectiviteit tot wel 75%.
Het onderzoeksteam is momenteel bezig met het verder uitwerken van hun ondervindingen en hopen hier een geschikte therapeutische en diagnostische toepassing voor te vinden.
Bron: Zhong, L. et al. (2025) Bioconjugate Chemistry, DOI: 10.1021/acs.bioconjchem.5c00167
















Nog geen opmerkingen