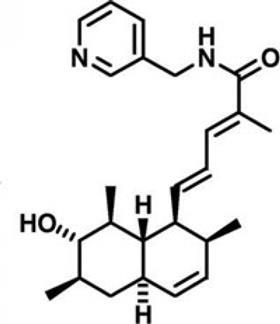
Japanse onderzoekers zijn er in geslaagd om (2E,4E)-5-((3S,4S,4aS,5S,6S,7R,8aR)-3,4,4a,5,6,7,8,8a-octahydro-6-hydroxy-3,5,7-trimethylnaftalen-4-yl)-2-methyl-N-((pyridin-3-yl)methyl)penta-2,4-dienamide te synthetiseren uit basisgrondstoffen. Ze zijn nu aan het uitzoeken of de verbinding zijn potentie als kankermedicijn kan waarmaken, schrijven ze in het Journal of Medicinal Chemistry.
Tot nu toe was de verbinding, die de werktitel AMF-26 heeft meegekregen, alleen gemaakt door modificatie van de aanverwante stof AMF-14. Die laatste wordt door het bedrijf Nippon Shinyaku geïsoleerd uit een Trichoderma-schimmel, maar kennelijk is de oogst onvoldoende om aan toepassingen als chemokuur te denken.
Intussen ligt er wel een publicatie over muizen, waarin menselijke borsttumoren waren getransplanteerd. Na orale toediening van AMF-26 gingen die tumoren weg.
Het is ook al duidelijk waardoor dat komt: AMF-26 blokkeert ADP-ribosyleringsfactor 1 (Arf1) en saboteert daardoor het Golgi-apparaat. Waarom vooral tumorcellen hier het slachtoffer van worden, wordt uit het verhaal dan weer niet duidelijk.
De totale synthese is een verhaal dat alleen voor doorgewinterde organici te volgen is. De belangrijkste stap is volgens de Japanners de selectieve vorming van een chirale lineaire precursor, ergens in het begin. Die stap kregen ze voor elkaar via een asymmetrische aldolreactie, gevolgd door een stereoselectieve intramoleculaire Diels-Alderreactie. Van te voren hadden ze via computersimulaties voorspeld dat ze het correcte stereo-isomeer zouden moeten krijgen, en in de praktijk bleek dat inderdaad te kloppen.
De eerste proefjes met een array van menselijke kankercellen hebben uitgewezen dat het volledig synthetische AMF-26 precies zo werkt als de uit AMF-14 afgeleide variant, en dat verschillende tumorcellijnen er door afsterven
bron: American Chemical Society















Nog geen opmerkingen