Les micro-particules d’hydrogel peuvent servir de véhicule pour mesurer les mouvements cellulaires en trois dimensions, comme le montrent des chercheurs de Wageningen. Comment les fabriquer et les utiliser est détaillé dans leur publication complète dans Nature Protocols.
Les cellules se déplacent lors de nombreux processus. Pour observer ces mouvements, une équipe internationale dirigée par le professeur Daan Vorselen (Wageningen UR) a développé des micro-particules d’hydrogel que l’on peut incuber avec les cellules. Cela permet de cartographier leurs déplacements en trois dimensions, ce qui n’était pas possible auparavant.
« Dans notre laboratoire, nous voulons comprendre le fonctionnement des processus immunitaires », explique Vorselen, bio-physicien de formation. Il utilise des stratégies chimiques pour évaluer la réponse des cellules immunitaires. « Nous examinons comment elles interagissent avec des cibles de différentes formes et tailles et comment cela influence leur comportement. »
Ingérer
Le principe appliqué par Vorselen et ses collègues consiste à utiliser les hydrogels pour suivre les mouvements. « Dans le domaine de la biophysique, cette technique est surtout utilisée pour observer les cellules sur une surface plane. » On fabrique d’abord un hydrogel contenant des nanoparticules. Lorsque la cellule se déplace dessus, le gel se déforme et les nanoparticules bougent. À partir des propriétés mécaniques du gel, il est possible de calculer les forces et déplacements.
« Cette approche fonctionne aussi pour les cellules immunitaires », poursuit Vorselen. « Une cellule immunitaire ne peut pas simplement interagir avec une surface plane. Nous nous sommes demandé si cela ne pourrait pas fonctionner avec de petites billes. »
Capteurs de force
La mise en œuvre a demandé de relever plusieurs défis. « Nous devions maîtriser la synthèse des micro-particules et la manière d’extraire les forces à partir des déformations », raconte Vorselen. Les extrêmes, particules de 100 µm et plus ou nanoparticules, sont assez simples à produire. « Nous voulions des particules de 10 µm ou moins, ce qui est plus complexe. » Grâce à un procédé d’émulsification et à une membrane microfluidique multicanaux fournie par SPG Technology, ils ont produit des milliards de billes uniformes.
Ces billes servent de capteurs de force. « Ce n’est pas une question chimique mais d’élasticité », précise Vorselen. « Si l’on comprime ou étire une bille, elle conserve pratiquement la même forme. Comment alors calculer les forces exercées uniquement à partir de la forme ? Nous avons collaboré avec des ingénieurs de Stanford, Yifan Wang et Wei Cai, pour trouver la solution. »
Un coup de chance
Ils ont également bénéficié d’une avancée précieuse. Vorselen : « Il fallait déterminer la rigidité optimale pour que la bille se déforme correctement et puisse interagir avec la cellule immunitaire. Notre première estimation était parfaite. » Cela a accéléré le processus.
Ce n’est qu’en observant les déformations au microscope que les chercheurs ont compris que la méthode fonctionnerait. « Jusqu’alors, c’était hypothétique. Cela s’appuie sur mon travail postdoctoral avec Julie Theriot à l’Université de Washington et il faut reproduire les résultats dans d’autres laboratoires. Nos doctorants Alvja Mali et Youri Peeters ont réussi, ce qui nous a permis de publier un protocole complet pour aider d’autres équipes. »
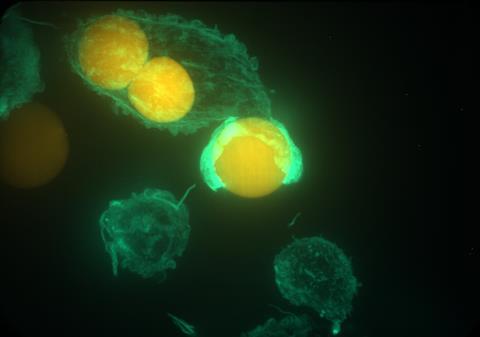
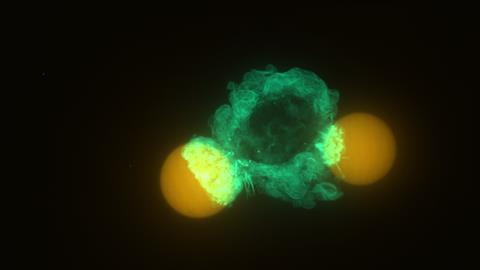
Cette technique permet de mesurer les forces parallèles à la surface et les forces normales, ce qui n’était pas accessible auparavant. Vorselen : « Nous observons que les cellules compressent les billes comme un serpent ou un cordage qui s’enroule. Ce comportement est inattendu et reste à expliquer. »
Biomarqueur
Les applications sont prometteuses. « Par exemple comme outil de criblage », indique Vorselen. « D’autres travaux ont montré que plus une cellule immunitaire exerce de force, plus elle est efficace pour détruire les cellules cancéreuses. La force pourrait servir de biomarqueur pour évaluer l’efficacité. »
Pour cela, il faudra augmenter la cadence. « Aujourd’hui, analyser une cellule prend un quart d’heure. Pour accélérer, il serait possible de simplifier certaines mesures et de collecter moins de détails afin d’obtenir des résultats plus rapides. »
Mali, A., Peeters, Y. et al. (2025) Nat Protoc, DOI: 10.1038/s41596-025-01281-2
Les cellules se déplacent lors de nombreux processus. Pour observer ces mouvements, une équipe internationale dirigée par le professeur Daan Vorselen (Wageningen UR) a développé des micro-particules d’hydrogel que l’on peut incuber avec les cellules. Cela permet de cartographier leurs déplacements en trois dimensions, ce qui n’était pas possible auparavant.
« Dans notre laboratoire, nous voulons comprendre le fonctionnement des processus immunitaires », explique Vorselen, bio-physicien de formation. Il utilise des stratégies chimiques pour évaluer la réponse des cellules immunitaires. « Nous examinons comment elles interagissent avec des cibles de différentes formes et tailles et comment cela influence leur comportement. »
Ingérer
Le principe appliqué par Vorselen et ses collègues consiste à utiliser les hydrogels pour suivre les mouvements. « Dans le domaine de la biophysique, cette technique est surtout utilisée pour observer les cellules sur une surface plane. » On fabrique d’abord un hydrogel contenant des nanoparticules. Lorsque la cellule se déplace dessus, le gel se déforme et les nanoparticules bougent. À partir des propriétés mécaniques du gel, il est possible de calculer les forces et déplacements.
« Cette approche fonctionne aussi pour les cellules immunitaires », poursuit Vorselen. « Une cellule immunitaire ne peut pas simplement interagir avec une surface plane. Nous nous sommes demandé si cela ne pourrait pas fonctionner avec de petites billes. »
Capteurs de force
La mise en œuvre a demandé de relever plusieurs défis. « Nous devions maîtriser la synthèse des micro-particules et la manière d’extraire les forces à partir des déformations », raconte Vorselen. Les extrêmes, particules de 100 µm et plus ou nanoparticules, sont assez simples à produire. « Nous voulions des particules de 10 µm ou moins, ce qui est plus complexe. » Grâce à un procédé d’émulsification et à une membrane microfluidique multicanaux fournie par SPG Technology, ils ont produit des milliards de billes uniformes.
Ces billes servent de capteurs de force. « Ce n’est pas une question chimique mais d’élasticité », précise Vorselen. « Si l’on comprime ou étire une bille, elle conserve pratiquement la même forme. Comment alors calculer les forces exercées uniquement à partir de la forme ? Nous avons collaboré avec des ingénieurs de Stanford, Yifan Wang et Wei Cai, pour trouver la solution. »
Un coup de chance
Ils ont également bénéficié d’une avancée précieuse. Vorselen : « Il fallait déterminer la rigidité optimale pour que la bille se déforme correctement et puisse interagir avec la cellule immunitaire. Notre première estimation était parfaite. » Cela a accéléré le processus.
Ce n’est qu’en observant les déformations au microscope que les chercheurs ont compris que la méthode fonctionnerait. « Jusqu’alors, c’était hypothétique. Cela s’appuie sur mon travail postdoctoral avec Julie Theriot à l’Université de Washington et il faut reproduire les résultats dans d’autres laboratoires. Nos doctorants Alvja Mali et Youri Peeters ont réussi, ce qui nous a permis de publier un protocole complet pour aider d’autres équipes. »
Cette technique permet de mesurer les forces parallèles à la surface et les forces normales, ce qui n’était pas accessible auparavant. Vorselen : « Nous observons que les cellules compressent les billes comme un serpent ou un cordage qui s’enroule. Ce comportement est inattendu et reste à expliquer. »
Biomarqueur
Les applications sont prometteuses. « Par exemple comme outil de criblage », indique Vorselen. « D’autres travaux ont montré que plus une cellule immunitaire exerce de force, plus elle est efficace pour détruire les cellules cancéreuses. La force pourrait servir de biomarqueur pour évaluer l’efficacité. »
Pour cela, il faudra augmenter la cadence. « Aujourd’hui, analyser une cellule prend un quart d’heure. Pour accélérer, il serait possible de simplifier certaines mesures et de collecter moins de détails afin d’obtenir des résultats plus rapides. »
Mali, A., Peeters, Y. et al. (2025) Nat Protoc, DOI: 10.1038/s41596-025-01281-2












Nog geen opmerkingen