Onderzoekers van de VUB en de University of the Free State (Zuid-Afrika) presenteren in European Journal of Organic Chemistry een nieuwe fluorescente peptide hydrogel met makkelijk aanpasbare sequenties. Dat biedt zicht op doelgerichte, moduleerbare medicijnafgiftesystemen.
Hydrogelen zijn vanwege hun unieke eigenschappen aantrekkelijke biomaterialen voor de gecontroleerde afgifte van geneesmiddelen. Onder invloed van druk wordt zo’n gel vloeibaar genoeg om subcutaan te injecteren, maar vrijwel onmiddellijk daarna vormt het weer een gel. Vervolgens erodeert deze gel langzaam, waardoor de opgeslagen biologisch actieve bestanddelen traag kunnen vrijkomen. Onderzoekers aan de Vrije Universiteit Brussel (VUB), waaronder de groep van chemici Steven Ballet, Charlotte Martin en Ulrich Hennecke, werken aan hydrogelen die uit natuurlijke peptiden bestaan en daardoor makkelijk afbreekbaar zijn in het lichaam.
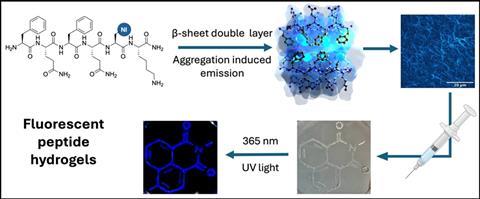
Voor de ontwikkeling van deze peptide hydrogels werken de VUB-onderzoekers aan de synthese van gemodificeerde aminozuren die bepaalde eigenschappen met zich meebrengen. Deze aminozuren plaatsen ze vervolgens in een peptidesequentie waarvan bekend is dat deze assembleert tot een hydrogel. Nu hebben ze, geholpen door wat serendipiteit, een nieuw aminozuur ontwikkeld op basis van 1,8-naphthalimide dat een fluorescente peptide hydrogel vormt, met versterkte emissie na aggregatie. Steven Ballet, hoogleraar organische chemie, legt uit: ‘Onze gebruikte peptidesequentie bestond voorheen onder meer uit fenylalanines die zelfassembleren tot bèta-sheet structuren. Maar toen we de zijketens van de aminozuren veranderden, ontdekten we dat de gels fluorescent werden.’
Bij toeval
De peptidesequentie waar de onderzoekers mee werken bestaat uit aminozuren met hydrofobe benzeenringen aan dezelfde zijde van de keten. Deze aromatische zijketens associëren met elkaar, wat zorgt voor de vorming van peptidevezels en bijgevolg een stabiele hydrogel. Oorspronkelijk zochten Ballet en collega’s naar manieren om de stabiliteit verder te verhogen en nog sterkere vezels te maken. ‘We wilden de aromaten door grotere hydrofobe polycyclische systemen vervangen om nog meer stabiliteit te creëren’, zegt Ballet. ‘Een beetje bij toeval ontdekten we dat sommige van onze vervangingen ervoor zorgden dat de ketens fluorescent werden.’
Die toevallige ontdekking kwam de onderzoekers goed uit. Hun hoofddoel is namelijk om gecontroleerde afgiftesystemen te ontwikkelen met moduleerbare eigenschappen. Met de toegevoegde eigenschap van fluorescentie is de gel zichtbaar na subcutane injectie. ‘Dat is handig voor beeldvorming, willen we de lokalisatie van de gelen na injectie onderzoeken’, zegt Ballet. ‘Nu kunnen we wel tien tot twintig dagen in vivo opvolgen hoe lang de gel op de plaats van injectie blijft en hoe snel ze eroderen. Dat geeft ons nodige inzichten om betere systemen te ontwikkelen.’
Versterkte emissie
De onderzoekers synthetiseerden hun aminozuren onder meer met palladium-gekatalyseerde koppelingsreacties. Door deze aminozuren vervolgens in de peptidesequentie in te bedden, trad de fluorescentie pas echt duidelijk naar voren. De vorming van bèta-sheet structuren bepaalde hierbij de oriëntatie van de lichtgevende zijketens en zorgde ervoor dat de emissie na aggregatie toenam.
‘Binnen deze studie vormde de aanmaak van de aminozuren het grootste werk’, zegt Ballet. ‘Hierbij was onzeker welke materiaaleigenschappen zouden ontstaan. Maar dat is tegelijk de schoonheid van organische chemie: dat je moleculen kan blijven aanpassen naar wat je wilt. Zodra je een lead hebt, kan je de structuren steeds verder ombouwen om de eigenschappen van de peptideketen bij te schaven.’
Antilichamen
Op weg naar gecontroleerde afgiftesystemen hopen de onderzoekers nog meer grip te krijgen op hun biomaterialen. Zo geven hun huidige peptide gels het actieve bestanddeel de eerste drie tot zeven dagen na injectie vrij, wat ze minder langdurig maakt dan gels met synthetische polymeren. Ballet: ‘Maar dankzij de moduleerbaarheid van onze peptiden kunnen we relatief snel nieuwe systemen ontwikkelen door de structuren aan te passen. Zo willen we komen tot sterkere materialen met een tragere afbraak in het lichaam.’
Daarnaast willen de onderzoekers de compatibiliteit tussen de actieve bestanddelen en de materiaaleigenschappen van de hydrogel verder bestuderen. In het verleden lieten ze al zien hoe hun hydrogel geschikt was om kleine moleculen, peptiden en nanobodies (kleinere varianten van antilichamen) vrij te geven. ‘Maar dat beslaat nog niet het hele spectrum aan mogelijke medicijnen’, aldus Ballet. ’Zo zijn we nu aan het kijken of ons systeem ook grote antilichamen kan vrijgeven. Dat is het mooie aan ons systeem: in plaats van beperkt aanpasbare synthetische polymeren is onze gel veelzijdig en om te bouwen tot een “vriendelijker” omgeving voor therapeutische eiwitten.’
Jolien Bertouille, Adelaide R. Mashweu, et al., Fluorescent β-sheet-based peptide hydrogels with aggregation-enhanced emission properties, EurJOC (2025), doi:10.1002/ejoc.202500730

















Nog geen opmerkingen