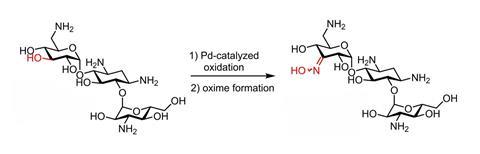
Als je de aminegroep op een suiker eerst protoneert, kun je met palladium zonder verdere beschermgroepen selectief een van de hydroxygroepen oxideren, laten Nederlandse en Zwitserse onderzoekers zien in Chemistry A European Journal.
In de organische synthese kom je niet ver zonder beschermgroepen: het ene reactieve of gevoelige deel van je molecuul heeft bescherming nodig, zodat een andere reactieve groep kan reageren. Al dat beschermen kost tijd en moeite, en kan bovendien de opbrengst verminderen. Ook de suikerchemie heeft hier last van, maar de groepen van Adri Minnaard en Martin Witte van de Rijksuniversiteit Groningen en collega’s uit Zürich laten nu zien hoe je aminoglycanen selectief op C3 kunt oxideren zonder beschermgroepen.
Dat je die C3-positie selectief kunt oxideren met een palladiumkatalysator was al bekend. De onderzoekers verwijzen naar eerder werk waarin ze precies dat doen, maar dan met een beschermgroep op het primaire amine op de C6-positie. Dat komt omdat die zijgroepen zich gedragen als een Lewisbase, waar de katalysator een Lewiszuur is. Zodoende inhibeert de zijgroep de katalysator waardoor die zijn werk niet meer kan doen.
Voeg je echter een Brønstedzuur toe voordat je de katalysator toevoegt, dan protoneer je de aminegroep, waardoor die niet meer reageert met de katalysator. Dit is dan ook wat de onderzoekers laten zien in deze paper, eerst met monosachariden ter demonstratie, maar vervolgens ook met trisachariden. In methanol met trifluormethaansulfonzuur (TfOH) ging dat het beste.
De onderzoekers brachten deze methode direct in de praktijk door Kanamycine A-varianten te maken. Kanamycine A, een antibioticum, is een trisacharide met zo’n primair amine op de C6-positie. Nu blijft resistentie tegen dit soort antibiotica de kop opsteken, dus als je gemakkelijk variaties kunt maken op zulke middelen, heb je een grotere kans op het vinden van een variant die de opgebouwde resistentie tegen een middel omzeilt.
Voor de varianten gold dezelfde syntheseprocedure: de trisacharide – met allerlei onbeschermde hydroxy- en aminegroepen – protoneer je met zuur en oxideer je met de katalysator. Op die manier maakten ze allerlei varianten die ze ook testten. Hoewel de meesten niet per se beter werkten dan origineel Kanamycine A in normale bacteriën, was dat wél het geval bij gemuteerde bacteriën die resistentie nabootsten.
Het mooie van dit werk is de enorme winst die ze behaalden in reactiestappen. De traditionele manier van oxideren gaat in elf stappen – waarvan tien bescherm- en ontschermstappen en slechts één stap voor het oxideren. In deze nieuwe procedure heb je alleen de oxidatiestap. Ook verbeterden ze een eerder protocol voor een van de varianten: waar ze eerst een totale opbrengst van 10% over vier stappen hadden, haalden ze nu 58% over twee stappen. Het biedt al met al een interessante tool voor de chemische biologie en op aminoglycoside gebaseerde antibiotica.
Marinus, N. et al. (2024) Chem. Eur. J. e202400017, DOI: 10.1002/chem.202400017




















Nog geen opmerkingen